Hyaluronate de sodium à usage pharmaceutique
-

-
Fabriqué intégralement au Japon, ce produit offre une qualité constante et une pureté élevée.
Ce hyaluronate de sodium à usage pharmaceutique est conforme aux réglementations pharmaceutiques mondiales.
Fabrication intégrale dans notre usine nationale

Dérivé de la fermentation microbienne, d’origine non animale, sans OGM

. Il s'agit d'une substance macromoléculaire extracellulaire dérivée de Streptococcus zooepidemicus, une souche de bactéries lactiques.
Conformité avec les réglementations pharmaceutiques mondiales
L’hyaluronate de sodium est conforme aux réglementations pharmaceutiques mondiales et est très apprécié en tant que fournisseur d’API sur les marchés européen, américain, japonais, coréen et indien.
Il répond également aux normes officielles de ces pays et régions, et possède les enregistrements pharmaceutiques ainsi que les autorisations d’exploitation.
Informations sur les enregistrements pharmaceutiques et les autorisations d’exploitation par pays et régions
| Pays/Région | Enregistrement pharmaceutique et autorisation d’exploitation | Autorité réglementaire |
|---|---|---|
| L'Union européenne |
Certificate of Suitability to the European Pharmacopoeia | EDQM |
| États-Unis | Drug Master File for US FDA | FDA |
| Corée du Sud | Drug Master File | MFDS |
| IInde | API Registration Certificate | CDSCO |
| Japon |
Master file |
PMDA |
Conformité avec les normes officielles des pharmacopées des différents pays et régions
| European Pharmacopoeia | Sodium Hyaluronate |
|---|---|
| Japanese Pharmacopoeia | Purified Sodium Hyaluronate |
Certification Halal obtenue

Notre hyaluronate de sodium, produit par fermentation microbienne est certifié HALAL (Malaisien JAKIM) par l’Association Musulmane du Japon (JMA).
Large gamme de poids moléculaires (viscosités), permettant une application variée dans les formulations
Avec une large gamme de poids moléculaires (de hauts à faibles) et de viscosités (de fortes à légères), nous offrons des produits adaptés à de nombreuses formulations pharmaceutiques (FDF).
|
Product Name |
SODIUM HYALURONATE | |||||
|---|---|---|---|---|---|---|
| Pharma Grade 80 | GS-40 | GS-100 | GS-120 | GS-200 | GS-300 | |
| Intrinsic Viscosity (m3/kg) |
1.55–2.00 | 0.39-0.99 | 1.00–2.49 | 1.5-2.0 | 2.50–3.31 | 3.32-4.60 |
| Shelf Life | 3 Years* | 2 Years* | 3 Years* | |||
| Storage Conditions | 2 to 8℃ | -25 to -15℃ | ||||
| Packaging | 100g | 100g, 200g | 100g | |||
| Bacterial Endotoxins (EU/g) |
Not more than 2.5** | Not more than 40** |
Less than 50** | Not more than 40** | Less than 50** | |
Les valeurs ci-dessus sont données à titre indicatif. Veuillez demander le cahier des charges pour les spécifications officielles. Ces données peuvent ne pas correspondre à l’ensemble des enregistrements réglementaires (MF, etc.), lesquels varient selon les produits.
Si nécessaire, une adaptation dans le cadre des limites spécifiées est possible sous contrat GQP.
* Période de garantie : basée sur la viscosité intrinsèque (I.V.) mesurée au moment de la fabrication pour chaque grade.
** Norme EP : limite inférieure à 0,05 (EU/mg).
Utilisable comme ingrédient actif (API) ou excipient dans les médicaments et les dispositifs médicaux
-
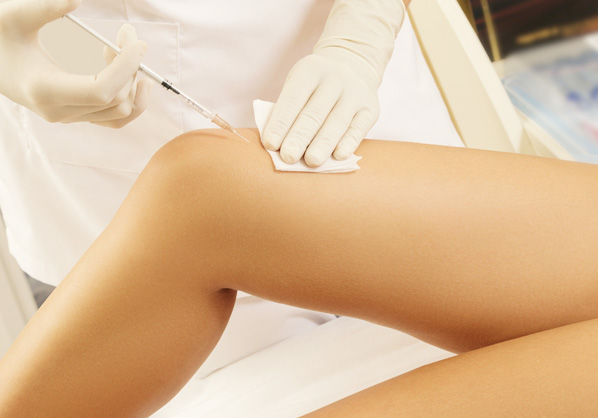
Injections articulaires
Solutions injectables pour le genou
(arthrose, polyarthrite rhumatoïde) /
Régénération osseuse -
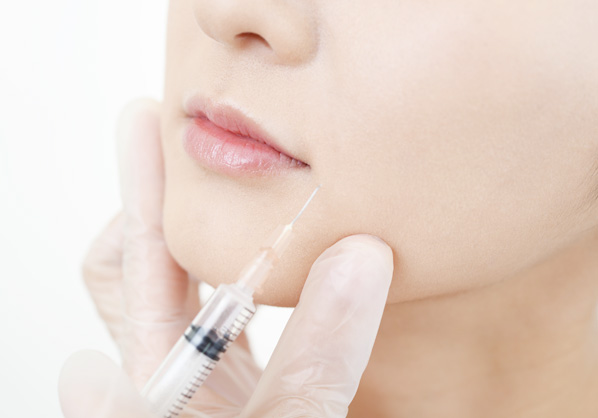
Chirurgie esthétique
Produits de comblement dermique /
Remodelage des contours /
Correction de la silhouette -
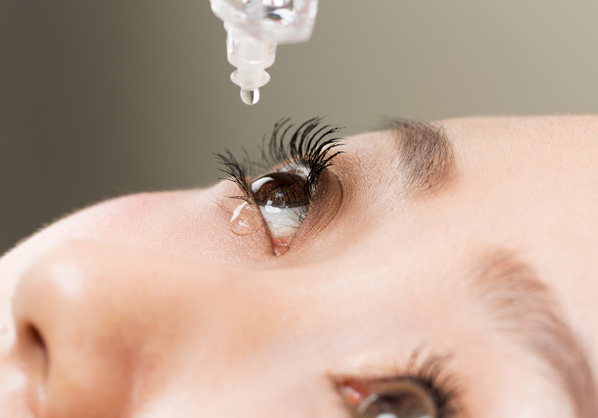
Ophtalmologie
Viscoélastiques ophtalmiques (OVD) /
Collyres /
Produits d’entretien pour lentilles de contact /
Dispositifs d’insertion d’implants intraoculaires -

Usage externe
Soins de la peau /
Produits dermatologiques /
Traitements pour lésions cutanées -
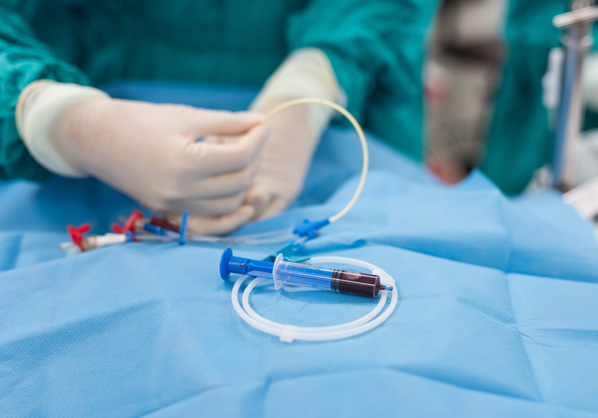
Dispositifs médicaux
Endoscopes, agents de revêtement pour cathéters /
Agents anti-adhésion /
Traitement du reflux vésico-urétéral /
Résection de la muqueuse colique (EMR)
Contact
Demande de documentation : Si vous êtes intéressé, n’hésitez pas à nous contacter pour demander un catalogue, des spécifications, des fiches de données de sécurité ou des échantillons.
